microRNA(miRNA)是一种机体内源性表达的单链小分子RNA,位于基因组非编码区,本身不具有开放阅读框(open readingframe,ORF),具有高度保守性,时序性和组织特异性。miRNA广泛存在于各种真核细胞中,不编码任何蛋白质,长度仅为20~24nt。成熟的miRNA5′端有一个磷酸基团,3′端为羟基,由具有发夹状结构的约70~90nt的单链RNA前体经过Dicer酶加工后形成。成熟的miRNA形成RNA诱导的基因沉默复合体(RNA-inducedsilencing complex,RISC)作用于靶点mRNA,通过对mRNA剪切或抑制其翻译过程而调控基因的表达。目前人们还不明确miRNA及其靶mRNA之间的作用机制。
最近有研究指出,miRNA在细胞生长、发育、分化、死亡等生物过程中起着重要的作用,同时,miRNA参与了血细胞生成、胰岛素分泌、神经系统构成和人类癌细胞生长等不同的过程,因此,非常有必要开发有效的实验工具来测定miRNA。
目前检测miRNA的方法主要有Northern印迹分析,微点阵(microarray)分析和实时定量PCR(quantitativeReal-TimePCR)。下面将对这三种方法做简单的介绍及比较。
1、Northern印迹分析(Northern Analysis)
Northern印迹是基于杂交检测RNA的常用方法,它是最早用于miRNA分析的几种方法之一。这种方法简单易行,大部分实验室都可以进行操作,不需要额外的资金投入与设备更新。
不足之处:
1)Northern分析的过程涉及大量人工操作,并且每次仅有一条miRNA探针与一个RNA印迹杂交,因此,它适用于不适用于大规模的筛选实验。尽管如此,在简单探究miRNA功能机理的实验中,Northern印迹分析还是能够满足研究需要的。
2)Northern印迹分析的动态范围只能达到两个数量级,这就引发了一个严重的问题,进行实验的细胞内的miRNA分子的数量要达到比较大的范围,例如,能够检测40,000个miRNA分子每细胞的印迹条件实际上却不能准确检测10个miRNA分子每细胞。另外,由于Northern印迹以杂交为原理,它通常不能有效区分具有细微序列差异的miRNA。例如,同一个家族中的miRNA let-7c与let-7a和let-7b之间仅有一个碱基的差异,导致Northern印迹分析无法清晰区分它们。此外,Northern印迹实验的重复性较弱。
3)Northern印迹耗时,耗量。进行一次miRNA检测需要3个工作日,不仅减慢了实验进程,也增加了杂交膜上信号扩散的风险。此外,Northern印迹大概需要5到10微克的总RNA量上样量才能成功检测出miRNA,增加了检测干细胞或人类初期肿瘤细胞这些稀少的样品的难度,甚至无法顺利开展实验。
2、微点阵(Microarray)分析
微点阵分析也是基于杂交的原理来检测miRNA,它通过测定特定过程中miRNA的表达水平,来分析了解miRNA的表达调控机制以及由miRNA调控的基因的表达。微点阵采用高密度的荧光标记探针与RNA样本杂交,通过荧光扫描获得表达图谱,借助相应软件进行miRNA的表达分析。由于在设计探针时可以包含所有可用miRNA序列,因此微点阵可以作到高通量的miRNA分析。
不足之处:
1)微点阵仍然需要足够的RNA初始样本,大约为每个微点阵5微克。
2)由于微点阵以杂交为基础,因此同Northern印迹一样无法清楚的区分序列差异很小的miRNA。另外,微点阵也很难区分具有相同序列的前体miRNA和成熟的活性miRNA。
3、定量实时PCR(Quantitative Real-time PCR)
定量实时PCR技术通过扩增技术,是指在PCR反应体系中加入荧光基团,利用荧光信号积累实时监测整个PCR进程,最后通过标准曲线对未知模板进行定量分析的方法。起始目标核酸的拷贝数越高,就越快观察到荧光强度的显著增加。定量实时PCR中TaqMan
尽管定量实时PCR相比Northern分析和微点阵需要较少的样本,并且显著的提高了动态范围和敏感度,但是这种技术在检测miRNA时还是遇到了挑战。由于成熟miRNA长度较短,难以设计成熟miRNA的有效的特异引物和探针,于是很多研究者对较长的前体miRNA分子进行定量实时PCR检测,利用前体miRNA的水平作为成熟的活性miRNA的替代标记。然而细胞内存在的前体miRNA的水平不能有效的指示相应的成熟miRNA水平,因此这种方法无法达到预想中的效果。
目前已有新的定量实时PCR的方法被用来解决检测miRNA中遇到的这些问题。这种新方法利用一种茎环(stem-loop)状引物进行miRNA的反转录,然后再进行定量实时PCR。这个茎环状结构对成熟的miRNA3′ 端具有特异性,能够将非常短的成熟miRNA分子扩展并且增加一个通用的3′ 引物位点进行实时PCR。这种茎环状结构也被认为可以形成一种空间的阻碍以防止对前体miRNA进行PCR引导。然后就可以利用实时PCR进行高特异性的定量检测miRNA的表达水平。这种实时PCR的优点是:1)可以在起始样本量很小的情况下进行(RNA总量在1到10ng之间)。2)动态范围达到了7个数量级,因此可以检测大量或者少量的miRNA。3)这种方法可以区分只有一个碱基差别的miRNA。4)和传统的定量实时PCR检测相比,在实验室中生产这些新的茎环状结构是很快并且很简单的。5)但也很多的不足之处,对于比较珍贵的标本,反转录一次,无法对其产物进行检测有很大的局限性。
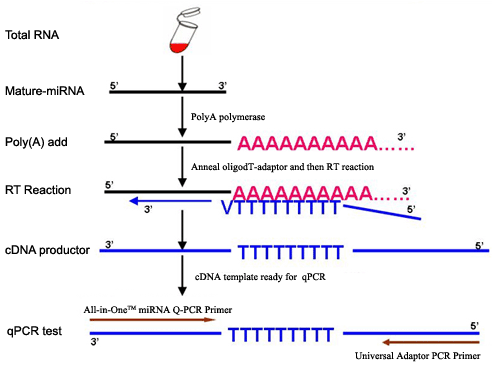
通过Poly A Polymerase 对miRNA 3’端进行加“Poly A”处理,同时利用M-MLV RTase 及独特的OligodT Adaptor 对Poly A 化的RNA 进行反转录,最后采用含有SYBR Green 的Q-PCR Mix对miRNA 进行特异性检测。
三种检测方法的比较
1. 检测简便、快捷、节约:miRNA qPCR Detection System是基于SYBR Green染料法的qPCR检测系统,可用于从一个合成反应的cDNA中检测多种miRNAs,不仅减少了误差、节约了样品,同时还实现了检测的高通量
2. 检测的特异性:独特的miRNA引物设计技术及其优化的反应体系避免了非特异性扩增、特别是Pre-miRNA的污染
3.检测分辨率高:该系统能分辨单碱基差异的miRNA
4.一站式解决方案:公司不仅提供检测的试剂盒,还提供经验证的人源、小鼠源、大鼠源的特异性miRNA 检测引物。
5.检测灵敏度高:可在低至pg级的总RNA中检测到特异表达的miRNA
参考文献:
[1]Yingqing S, Seongjoon K, Neill W, et al.Development of a micro-arrayto detect human and mouse microRNAs and characterization of expressionin human organs. Nucleic Acids Res,2004,32
[2]Caifu C, Kelly M, Ada H.W, et al. Real-time PCR:Advancing RNAInterference and MicroRNA Studies. Nucleic Acids Research, 2004,32,
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享