随着亲和层析技术的发展,蛋白纯化技术相对简单,蛋白纯化技术的应用也越来越普遍,一步亲和层析即可达到90%以上的纯度。然而,蛋白纯化的过程中各个环节不容忽视。样品处理,纯化介质的选择,纯化方法的考虑,等等,虽然纯化方法简单,但是蛋白不同,采用的纯化体系也不尽相同。只要达到最终的纯化目的就是最好的纯化方法。
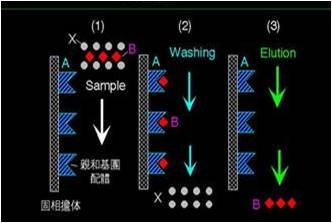
对于亲和层析纯化抗体,不论是蛋白A/G还是特异性抗原亲和层析,酸洗脱峰后一般加Tris中和。因为蛋白长期在酸性条件下易水解。但有一个问题就是中和容易产生沉淀。这是为什么?是抗体变性了?如何才能避免这种情况呢?
这种沉淀主要是因为洗脱时的酸性条件导致抗体变形,而在中和的时候,pH的剧烈变化更易导致抗体的变性。沉淀发生的另一个重要原因是宿主蛋白等杂质含量偏高。这类杂质在中和的时候容易导致溶液浑浊进而引发抗体沉淀。
要减少沉淀的发生应该从几个方面入手:
(1)尽量提高洗脱液的pH值。了解蛋白pH稳定性,包括低pH的稳定性,以及抗体的溶解度。如果pH稳定性低,最好使用Mabselect Sure探索高PH洗脱(PH5.0,4.0,3.0),都可以去尝试。高PH可以洗脱的,尽量不要选择更低的PH。
(2)尽量减少宿主蛋白。可以在亲和层析之前经过深层过滤,絮凝沉淀,超滤等方法去掉一些宿主蛋白类杂质。另外优化亲和层析时的中间洗涤步骤,尽量更多的去除宿主蛋白。当然不同批次的料液,其宿主蛋白的含量有所不同,因此需要加强监控,控制好亲和层析上柱前的料液中HCP的含量。最好在上样后加wash 洗HCP,PH 6左右加添加剂wash更换)。另外,也有一些介质本身的HCP的非特异吸附(这种情况在文献中提到, agrose的非特异吸附少)
(3)同时可以添加一些尿素等变性剂以提高洗脱液的洗脱能力;也可以添加精氨酸等蛋白稳定剂,以减少蛋白的变形;也可以改善中和条件,中和用的tris溶液的浓度和用量不要太高(常用的是5%体积的1M tris)。如果是溶解度低的蛋白,适当降低亲和层析进样量;样品处理和纯化过程中,尽量保持较低的温度
(4)一般提纯后的蛋白,无论是溶液还是冻干,都是需要添加甘油或者醇类,糖类作为蛋白稳定的保护剂, 以免出现沉淀。
蛋白纯化是很多小伙伴比较关注的问题,以后本站还会继续跟踪分享一些热点问题,有需求的朋友可以留言比较关心的问题,本站会尽快回复解答,并希望可以集中一些热点问题进行分享,欢迎来踩~~~
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享

请问纯化后收集到的抗体溶液,加甘油或者醇类,糖类的话,浓度一般是加多少啦。
在亲和层析纯化抗体后,通常需要添加稳定剂以保护抗体免受降解。常见的稳定剂包括甘油、糖类(如蔗糖或海藻糖)、以及醇类(如乙醇)。添加这些稳定剂的目的是增加抗体的稳定性,特别是在长期保存或反复冻融过程中。以下是常用稳定剂的添加浓度建议:
1. 甘油
甘油常用于抗体溶液的冷冻保存,以防止冰晶形成和蛋白质变性。推荐添加浓度为:
最终浓度:10-50%
2. 糖类
糖类,如蔗糖或海藻糖,常用于增加蛋白质溶液的黏度和稳定性。推荐添加浓度为:
蔗糖
海藻糖
3. 醇类
醇类如乙醇(Ethanol)可以作为低浓度的防腐剂,但高浓度会导致蛋白质变性。推荐添加浓度为:
乙醇
添加方法:
准备稳定剂溶液:根据所需浓度配置稳定剂溶液。
混合:将稳定剂溶液缓慢加入抗体溶液中,轻轻混匀,避免剧烈振荡以防止抗体变性。
注意事项:
无菌操作:确保操作环境无菌,避免抗体溶液污染。
缓冲液匹配:添加稳定剂前,确保其与抗体溶液的缓冲液相容,以避免抗体失活或沉淀。
存储条件:根据稳定剂类型和抗体特性,选择适当的存储条件(如-20°C或4°C)。
通过合理添加稳定剂,可以有效延长抗体的保存期限,并维持其活性。